GMP洁净车间空气洁净度等级,“药品生产质量管理规范”(GMP)中规定:药品生产的洁净厂房内的生产环境参数如:温度和相对湿度以及压差等均是由生产工艺决定的,一般温度为18℃~24℃,相对湿度为45%~65%。在“药品生产质量管理规范”(GMP)的实施指南中规定的比较具体。即药品生产洁净厂房中的温度和相对湿度是以穿洁净工作服的操作人员不产生不舒服、不舒适为基准的。
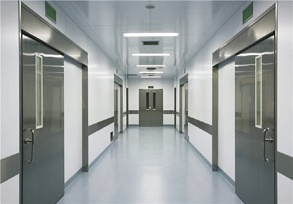
一、GMP无菌室实景图
二、净化工作原理
在特定的空间中,室内空气通过预过滤器进行预过滤,再由小型离心风机压入静压箱中,然后通过二级空气过滤器进行过滤,空气从空气过滤器中排出,吹净气流具有一定且均匀的截面风速,可以排出工作区域内的原始空气,带走灰尘颗粒和生物颗粒,形成无菌的高清洁工作环境。
三、技术要求及功能特点
技术要求:
洁净室的温度与相对湿度应与药品生产相适应;
保证一定的操作技术以及室内环境;
制定一定的管理制度;
不同洁净区之间一定要有过渡的缓冲室;
功能特点:
特殊性:净化厂房墙、顶板材一般多采用50mm厚的夹芯彩钢板制造,其特点为美观、刚性强、保温性能好、易施工。圆弧墙角、门、窗框等一般采用专用氧化铝型材制造;
防静电型:地面可采用环氧自流坪地坪或高级耐磨塑料地板,有防静电要求的,可选用防静电型;
阻燃型:送回风管道用热渡锌板制成,贴净化保温效果好的阻燃型PF发泡塑胶板;
美观性:高效送风口用不锈钢框架,美观清洁,冲孔网板用烤漆铝板。
四、应用场景
有盛净化GPM无菌室现广泛运用于实验室研究,微生物研究中,为了降低微生物和微粒污染的风险,实验与大多数产品应当在GPM无菌室进行,适用于过滤和灭菌。在获得无菌环境和无菌材料后,只有保持无菌状态,才能对已知的特定微生物进行研究。GPM无菌室的形成促进了科技事业的发展,也在一定程度上带动了生物制药的发展。





